La neuroprothèse
Introduction

Les chercheurs se sont imposés trois objectifs principaux dans leur démarche pour la récupération chez l'homme de la fonction motrice après des lésions de la moelle épinière. Ils visent ainsi l'autonomie du patient, la fluidité du mouvement et l'esthétisme du dispositif. Ce cahier des charges a axé les recherches des laboratoires vers la neuroprothèse à stimulation électrochimique. Bien que le terme "neuroprothèse" laisse suggérer un implant au niveau du cerveau, celle-ci se compose en fait de différents éléments répartis sur l'organisme ainsi que des appareils externes.
Comme dans la plupart des protocoles de recherche de cette envergure et avec de tels enjeux, les scientifiques ont tout d'abord effectué des expérimentations sur des animaux. Ainsi en 2012, une équipe de chercheurs de l'EPFL (Ecole Polytechnique Fédérale de Lausanne) sous la direction du Professeur Grégoire Courtine publiaient dans la revue Science des résultats convaincants sur les possibilités de rendre la mobilité à des rongeurs paraplégiques, avec un dispositif de neuroprothèse à stimulation électrochimique miniature, semblable à celui envisagé pour l'homme. Plus récemment, à Pékin, un consortium scientifique international dirigé par ce même Grégoire Courtine est parvenu à obtenir des résultats pertinents avec des tests encore plus poussés où des implants cérébraux ont été placé sur des primates paralysés dans le but de les rendre complètement autonomes dans leurs mouvements. En revanche l'opération sur le cerveau humain étant plus délicate et risquée que la première solution technique testée, les chercheurs ont plutôt poursuivi leurs recherches sur le dispositif de neuroprothèse à stimulation électrochimique utilisé sur les rats, pour une application à l'homme.
Quelle est la composition du dispositif de la neuroprothèse à stimulation électrochimique et quel est son fonctionnement ?
Composition
Le stimulus chimique
Pour effectuer la stimulation électrique sur les rats paraplégiques il a d'abord fallu réveiller les neurones de la moelle épinière ainsi préparer la coordination des mouvements des membres inférieurs. Les scientifiques ont alors premièrement stimulé la moelle épinière chimiquement, c'est à dire avec l'injection d'un cocktail de produits chimiques en dessous de la lésion.

Les substances injectées sont dites "agonistes de la monoamine", c'est à dire qu'elles lient les molécules de la Dopamine (Da), l’Adrénaline (A) et de la Sérotonine (5-HT). (voir partie Fonctionnement)
Schématisation de la stimulation chimique
L'injection se fait par l’intermédiaire de l'implant e-Dura sur lequel se trouve un canal pour micro-fluide assurant ainsi la stimulation chimique.
L'implant e-Dura
L'implant e-Dura est une prouesse technologique inventée par les équipes scientifiques de Grégoire Courtine et Stéphanie Lacour de l'EPFL. Cet implant neuronal, qui vient se placer sur la partie dorsale de la moelle épinière, tient sa particularité dans sa souplesse et son étirement. Ces caractéristiques qui le rapprochent des tissus vivants (comme la dure mère, membrane fibreuse de la moelle épinière) lui permettent d'être greffé directement sur la moelle épinière sans l'endommager, alors qu'une bande d'électrodes conventionnelle (rigide) à tendance à dégrader les tissus nerveux avec les frottements.


De plus l'implant est à la fois capable de délivrer des substances pharmacologiques, grâce à un canal, et des impulsions électriques par le biais d'électrodes. Il rend ainsi possible la stimulation chimique et électrique simultanément (stimulation électrochimique). Plus précisément, la stimulation électrique s'effectue à partir de signaux électriques qui sont envoyés par les électrodes dans la moelle épinière à partir des informations récupérées par l'accéléromètre.
Schématisation de l'implant e-Dura
Après deux mois d'utilisation de l'implant sur les rats, les résultats furent concluants puisque aucun rejet ni aucune lésion sur les tissus nerveux n'a été constaté. Les scientifiques projettent désormais des tests cliniques sur les humains.
L'accéléromètre
L'accéléromètre est un capteur permettant de mesurer l'accélération (changement de vitesse ou de direction) d'un objet.
Cette accélération peut être statique c'est à dire en fonction de l'inclinaison d'un objet (orientation de celui-ci par rapport à la Terre à partir de la gravité), ou dynamique liée aux mouvements. De plus, elle est basée sur la loi fondamentale de la dynamique suivante (deuxième loi de Newton) :

F = m.a
( F : force (N), m : masse (kg), a : accélération en m/s² )
L'utilisation d'accéléromètres est omniprésente dans notre quotidien notamment avec l'orientation des téléphones portables par rapport à la Terre (inclinaison) où le capteur permet à l'appareil de passer du mode portrait au mode paysage et inversement.

Dans le cadre de la neuroprothèse, l'accéléromètre, sous forme de caméras positionnées tout autour du sujet observé (pour les expérimentations avec les rats) ou sous forme de capteur placés directement sur le sujet (pour les hommes), enregistre les micros-mouvements volontaires du corps (provoqués préalablement par la stimulation chimique), ainsi que ses inclinaisons pour interpréter ses intentions de mouvements.
Enregistrement des mouvements d'un rat équipé d'une neuroprothèse à stimulation électrique (la ligne noire correspondant à l'axe de la patte du sujet)
Les ordinateurs
Le système informatique tient une place majeure dans le dispositif mis en place par les chercheurs. En effet, après que les caméras placées tout autour du sujet ou les capteurs (accéléromètre) aient enregistré tous les mouvements volontaires et informations sur le positionnement du corps de celui-ci, ces information sont envoyées aux ordinateurs qui par l’intermédiaire d'algorithmes vont les analyser, les traiter et les traduire en intentions de trajectoire.

Les informations ainsi interprétées, le système peut ensuite envoyer à des électrode ciblées un signal électrique pour que celles-ci renvoient des impulsions dans la moelle épinière. Ces dernières vont créer des mouvements du sujet (flexion ou extension).
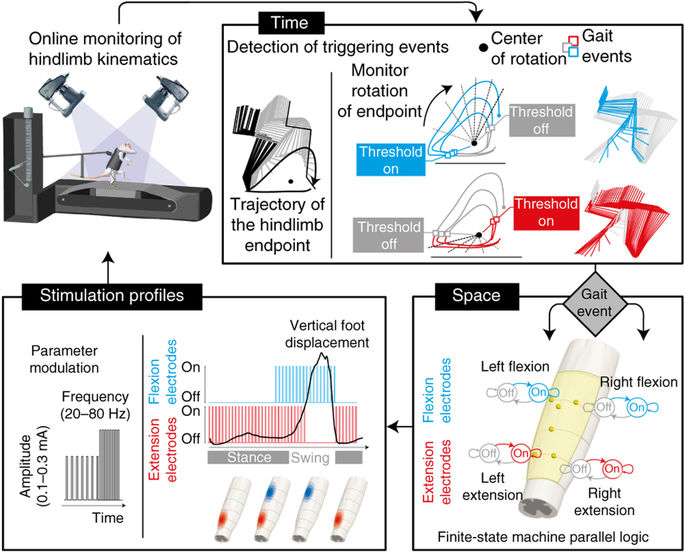
Informations recueillies par l'accéléromètre, analysées, traitées et renvoyées par les ordinateurs vers les électrodes
Le dispositif d'entrainement
Suite aux stimulations de la moelle épinière, le sujet doit réapprendre à marcher pour récupérer ses fonctions motrices. Il subit alors un entrainement où deux éléments majeurs interviennent : un tapis roulant et un harnais robotisé. Ce dernier a été créé par les équipes de scientifiques de l'EPFL, tout comme l'implant e-Dura. Il apporte un soutien vertical à l'individu sans pour autant lui faciliter le processus de marche. Ainsi celui-ci peut réapprendre à marcher en toute sécurité, tout d'abord sur tapis roulant, ensuite sur sol et enfin sur terrain avec des obstacles.

Fonctionnement
Les stimulations
Pour une récupération de la fonction motrice après une lésion de la moelle épinière chez un individu, la première étape consiste donc à réveiller la partie du système nerveux située sous la lésion. En effet, suite à cette lésion médullaire, la zone de la moelle épinière située sous celle-ci ne reçoit plus de message nerveux du cerveau et reste donc dans un état inactif, dit "de sommeil". Pour la réveiller on y effectue deux types de stimulation.

La première stimulation est chimique. Elle est effectuée avec l'injection d'un cocktail de produits pharmaceutiques dans la partie de la moelle épinière située sous la lésion. Cette administration se fait par l’intermédiaire de l'implant e-Dura (voir partie Composition). Ce cocktail est composé de différentes molécules dites "agonistes de la monoamine", c'est-à-dire des molécules de la Dopamine (Da), de l'Adrénaline (A) et de la Sérotonine (5-HT) qui sont liées entre elles. Ces molécules agissent comme des neurotransmetteurs, leur injection permet alors de réassurer la transmission de l'information entre les neurones de la partie de la moelle épinière sous la lésion (cf partie système nerveux). Ainsi cette première stimulation va permettre de réveiller en partie la moelle épinière du patient pour recréer partiellement l'apparition des mouvements volontaires.
Ces molécules stimulent les neurones en remplaçant les neurotransmetteurs normalement envoyés depuis le tronc cérébral (partie du système nerveux central) en passant par la moelle épinière (transmission impossible en cas de lésion). Les monoamines restaurent donc en partie les mouvements volontaires du sujet en réveillant la partie du système nerveux située sous la lésion.

Cette première stimulation chimique est complétée d'une seconde : la stimulation électrique. Grâce à ses interconnexions électriques et ses électrodes, l'implant e-Dura, placé sur la partie dorsale de la moelle épinière, envoi des impulsions électriques dans le système nerveux .
L'entraînement
Une fois la moelle épinière et les micro-mouvements volontaires en partie restaurés par les stimulations, vient l'étape de l'entraînement du sujet. En effet celui-ci doit réapprendre à marcher en effectuant des mouvements de flexions-extensions fluides. Pour cela l'individu est aidé par des machines et accompagné durant tout le processus, qualifié "d'entraînement" par les scientifiques en raison de l'effort physique considérable à produire.

Entrainement d'une personne paraplégique soutenue par le robot
Le sujet est soutenu par un robot-harnais qui le maintient en sécurité et le soulage sans lui faciliter la marche.
Grâce aux stimulations effectuées auparavant, le sujet est capable de produire des micro-mouvements avec ses membres inférieurs.
Les mouvements volontaires sont enregistrés par l'accéléromètre qui envoie ces informations aux ordinateurs.
Ces informations sont traduites par des algorithmes comme une volonté de mouvements. En fonction de ces volontés de mouvement, le système informatique, toujours par l’intermédiaire d'algorithmes, cible des électrodes précises (situées sur l'implant e-Dura) pour leur envoyer un signal électrique .
Ainsi, les électrodes envoient des impulsions électriques dans des endroits précis de la moelle épinière pour l'exciter de manière discontinue (courant phasique) ce qui crée une marche normale (flexion-extension).

Entraînement d'une personne paraplégique équipée de l'accéléromètre sur les jambes
L'impulsion électrique agit comme un message nerveux dans la moelle épinière (voir partie Système Nerveux). De ce fait, dès que l'individu veut lever le pied pour effectuer un pas, c'est à dire fléchir la jambe, l'ordinateur ne stimule alors que les électrodes qui sont responsables de la flexion de la jambe sur le muscle appelé ischio-jambier. Par ailleurs, dès que la personne veut poser le pied, l'ordinateur ne stimule que les électrodes responsables de l'extension de la jambe sur le muscle appelé quadriceps. Les électrodes n'agissant que sur les muscles concernés au bon moment, la marche devient alors de plus en plus fluide.
L'entrainement s'effectue tout d'abord sur tapis roulant (pour faciliter le mouvement de marche), puis sur sol, pour enfin évoluer sur des surfaces parsemées d'obstacles.
La Neuroplasticité
La neuroplasticité ou plasticité neuronale, peut se définir comme l'ensemble des manifestations traduisant la capacité des neurones à se remodeler tout au long de la vie. Ainsi, notre cerveau est en perpétuelle adaptation face à l'environnement et face aux différentes expériences qu'elles soient affectives, cognitives ou psychiques. Mais la plasticité neuronale peut aussi être remise en oeuvre suite à des lésions. Ici dans le cas de la paraplégie et de la lésion au niveau de la moelle épinière, la neuroprothèse est une méthode déterminante car elle induit la neuroplasticité. En effet, à force d'entraînements, les connexions entre les neurones se renforcent et se créent à nouveau, on parle alors de plasticité synaptique. Le but est alors que les malades, après de nombreux entraînements, puissent remarcher avec un déambulateur ou une canne et effectuer les actions simples du quotidien. En ce qui concerne la paraplégie et l'utilisation de cette neuroprothèse sur l'homme, un patient ne retrouvera certes jamais l'utilisation de ses jambes comme avant, mais c'est un progrès considérable pour son autonomie et pour les neurosciences.
